Актуальность исследований: Основной задачей растениеводства Самарской области является производство зерно и, в первую очередь, продовольственной пшеницы. Но в последние годы продуктивность этой культуры существенно снизилась. На низком уровне остается и качество зерна. По мнению ряда исследователей, урожайность яровой пшеницы в современных условиях может быть увеличено за счет применения биологических препаратов и регуляторов роста [7].
Изучение ростовых процессов, происходящих в растениях и механизмов их регуляции является одной из актуальнейших проблем современной физиологии растений. Особенно сложной представляется регуляторная система растений в результате действия на них стрессовых факторов среды. В литературе уже представлены сведения о негативном воздействии повышенной температуры на физиолого-биохимические процессы растительного организма, особенно на этапе прорастания. Выяснение причин потери жизнеспособности семян имеет не только теоретическое, но и важное практическое значение.
Однако применение биологически активных веществ, при возделывании яровой пшеницы в условиях Самарской области изучено не достаточно и нет конкретных рекомендаций по их применению.
Известно, что действие стрессовых факторов (повышенной температуры и высокой влажности воздуха) приводит к снижению жизнеспособности семян. Это выражается в уменьшении всхожести, изменении биохимического баланса выращенных из них проростков, снижению массы и линейных размеров данных проростков. Существуют многочисленные исследования, доказывающие, что экзогенное внесение фитогормонов может повысить жизнеспособность растений. Однако среди таких исследований немного работ, посвященных влиянию биологически активных веществ, внесённых экзогенно, на семена со сниженной жизнеспособностью. Между тем, такие исследования крайне актуальны и прежде всего для практического растениеводства, поскольку большие территории посевных площадей России расположены в местах «рискованного земледелия». Следовательно, разработка эффективных способов проращивания семени при неблагоприятных условиях поможет сохранить миллионы центнеров зерна для человечества.
Проблема исследования: Сегодня продолжается активный поиск новых синтетических регуляторов роста и изучение действия фитогормонов на растения. Представляет особый интерес выяснение роли фитогормонов в адаптационных реакциях. Большинство веществ, используемых в качестве фитогормонов мало токсичны для человека и животных. Хотя стоимость производства велика, экономический эффект, получаемый от их применения, может быть высок. Это положительное влияние фитогормонов проявляется при воздействии неблагоприятных факторов среды, что особенно важно в Самарской области, находящейся в зоне неустойчивого земледелия.
Цель работы: Изучить влияние экзогенно внесенных физиологически активных веществ на ростовые процессы яровой мягкой пшеницы сорта Кинельская Нива в ответ на действие стресса.
В соответствии с этим в задачи исследований входило:
1. Провести исследование снопового материала и определить структуру урожая яровой пшеницы по вариантам опыта;
2. Изучить влияние высокой температуры как стрессового фактора на ростовые процессы пшеницы;
3. Исследовать эффект стимулирующего действия предпосевной обработки семян пшеницы растворами биологически активных веществ в условиях термостресса.
Практическая ценность работы: Научная работа выполнялась совместно с кафедрой «Лесоводство, экология и безопасность жизнедеятельности» ФГБОУ ВПО Самарская ГСХА по программе НИР Министерства сельского хозяйства и продовольствия Самарской области (контракт № 16 от 08.08.2014 г). Полученные результаты будут использованы при разработке рекомендаций производству.
Концепция исследования: Повышенная температура оказывает негативное влияние на прорастание семян. Вероятным механизмом такого действия может быть изменение активности гидролаз – важных ферментов, преобразующих законсервированные соединения семян в рабочую форму. Особый интерес вызывала возможность оптимизации нарушенной активности данных ферментов в результате обработки семян экзогенно внесенными биологически активными веществами.
Объекты исследования: Физиологические особенности яровой мягкой пшеницы сорта Кинельская Нива.
Предмет исследования: Ростовые и продукционные процессы данного растения в зависимости от воздействия на семена перед посевом температурного стресса и БАВ.
Сформулирована гипотеза исследования: Воздействие на семена пшеницы повышенной температуры оказывает влияние на рост и развитие, растений. Обработка семян БАВ может помочь растению в постстрессовой реакции и снизить негативное воздействие данного фактора.
Новизна исследования: Сегодня все больше растительных объектов избираются для опытнической работы. Впервые изучено действие основных групп фитогормонов на яровую мягкую пшеницу.
Теоретическая значимость исследования: В настоящее время большое значение приобретают исследования, посвящённые изучению метаболизма различных сельскохозяйственных культур. Такие эксперименты позволяют расширить знания о разнообразии растений и физиологических процессах, протекающих под действием различных факторов среды.
Практическая значимость исследования: Материалы исследования могут быть использованы при организации мероприятий по рациональному использованию природных ресурсов.
Анализ исследований роли БАВ в стрессовой и постстрессовой реакции растений
Морфологические и биологические особенности пшеницы
Яровая пшеница – одна из древнейших наиболее распространенных культур на земном шаре. Она была известна более чем за 6,5 тыс. лет до н.э., за 6 тыс. лет до н.э. Ее с успехом выращивали в древнем Египте, Греции, в Римской империи. С давних времен выращивают пшеницу и в России. Возделывают ее во всех частях света – от полярного круга до крайнего юга Америки и Африки. Она является основной хлебной культурой большинства европейских стран, США, КНР, Японии, России, Казахстана, Украины. Яровая пшеница – ценная продовольственная культура. В зерне пшеницы содержится от 11 до 20 % белка, 63-74 % крахмала, около 2 % жиров, до 2 % зольных минеральных веществ и много витаминов (В1, В2, РР, Е, провитамины А, Д). Зерно яровой пшеницы отличается хорошими хлебопекарными свойствами. Пшеничный хлеб характеризуется высокой питательностью, вкусовыми качествами, а по усвояемости превосходит хлеб из муки других зерновых культур. В 100 г пшеничного хлеба содержится 245-255 ккал, что свидетельствует о высокой питательности и энергоемкости. Пшеничная мука кроме хлебопечения используется для производства макаронных и кондитерских изделий. Есть сорта, из зерна которых производят крупы (манная, перловая, ячневая). Зерно перерабатывают на спирт, крахмал, декстрин и т.п. Пшеница также используется в приготовлении пива и водки Отходы мукомольной промышленности (отруби) – ценный концентрированный корм для всех видов сельскохозяйственных животных. Солому в измельченном виде или сдобренную кормовой патокой используют как грубый корм для крупного рогатого скота. На корм скоту используется и полова [1]
Мировая площадь яровой пшеницы сейчас около 120 млн. га. Наибольшие площади ее посева находятся в России. По посевным площадям и валовому сбору зерна она занимает первое место среди других зерновых культур. Основные площади посевов яровой пшеницы сосредоточены в Нечерноземной зоне, Западной и Восточной Сибири, Поволжье, на Урале.
Из всего многообразия видов пшеницы в пищевой промышленности в настоящее время наиболее часто используется два основных вида: мягкая пшеница и твердая пшеница. Есть и другие виды, например, полба, ранее в силу своих ценных питательных качеств очень широко распространенная в России, а теперь используемая довольно редко [2]. Из мягкой пшеницы производится весь основной ассортимент булочных и кондитерских изделий. Наиболее дешевые виды макаронных изделий тоже делают из мягкой пшеницы. Из твердой пшеницы изготовляются макароны, булгур, кус-кус и твёрдые марки манной крупы. Содержание белка в зерне твердой пшеницы, как правило, превышает 20 процентов, что значительно больше, чем в зерне мягкой. В этом особая ценность твердой пшеницы. Она дает самую высококачественную муку – крупчатку. В хлебопечении ее используют в качестве улучшателя. Твердая пшеница выращивается в ограниченных районах земного шара с теплым и сухим климатом. В России яровая твердая пшеница высевается в Поволжье, на Южном Урале и в некоторых других районах. На мировом рынке наша твердая пшеница ценится особенно высоко[1],[2].
Яровая пшеница однолетние травянистые растения 40-150 см высотой. Корневая система мочковатая, располагается в верхнем пахотном слое почвы, но проникает на глубину 120-200 см. Она состоит из первичных «зародышевых» корней (развивается из зародыша семени) и вторичных «узловых» (образуются из узлов стебля). Стебель – соломина, по всей длине разделен узлами на 5-6 междоузлий. Листья ланцетовидные, с параллельным жилкованием, у основания свернутые в трубочки, прикрепленные к стеблевым узлам и охватывающие часть стебля. Размер и число листьев зависит от биологических особенностей, сорта и почвенных условий. Соцветие – сложный колос, состоящий из колосового стержня и отдельных колосков, содержащих 1-5 цветков, из которых зерно дают 2-3. Плод – голая зерновка (зерно), в котором различают спинную брюшную стороны. В нижней части зерна на спинной стороне расположен зародыш [8], [10].
Яровая пшеница – самоопыляющееся растение длинного светового дня. Она не предъявляет высоких требований к температуре. Мягкая пшеница более устойчива к низким температурам, чем твердая. Семена прорастают при 1-2 °С, а всходы появляются при 4-5 °С, наиболее благоприятная температура для прорастания – 12-15 °С. Яровая пшеница переносит непродолжительные заморозки (в период прорастания зерна -13 °С, а в фазу кущения -8-9 °С). Однако, во время цветения и налива зерна растения могут повредить заморозки в 1-2 °С. К высоким температурам довольно устойчива, особенно при наличии влаги в почве. Температура 35-40 °С и сухие ветры неблагоприятно сказываются на растениях и ведут к снижению урожайности и качества зерна [1], [11].
Для прорастания семян яровой мягкой пшеницы нужно 60-70 % воды от массы сухого зерна. Семена яровой твердой пшеницы требуют воды на 5-7 % больше, т.к. они содержат больше белка. Транспирационный коэффициент яровой мягкой пшеницы – 415ед, яровой твердой пшеницы – 406 ед. Наиболее благоприятная влажность почвы для яровой пшеницы – 70-75 %. Критическим периодом в потреблении воды считается фаза выхода в трубку и колошения, т.е. период образования репродуктивных органов. В этот период растениями потребляется 50-60 % всей необходимой воды.
К почвам яровая пшеница предъявляет высокие требования, особенно в начале вегетации к минеральному составу. У яровой пшеницы короткий вегетационный период и пониженная усваивающая способность корневой системы, поэтому наиболее благоприятными почвами для нее являются: черноземы, каштановые. А для мягкой яровой пшеницы – все виды черноземов, каштановых почв и серых слабооподзоленных темноцветных суглинков. На тяжелых глинистых и легких песчаных почвах без внесения высоких норм удобрений яровая пшеница растет плохо. Благоприятная pH – 6-7,5. Твердая пшеница предъявляет более высокие требования к плодородию, чистоте и структуре почвы, чем мягкая. В первый период жизни корни твердой пшеницы быстрее проникают вглубь, а у мягкой – энергичнее распространяются в ширину [17].
Из особенностей биологии яровой пшеницы следует отметить недружность и изреженность ее всходов. Причинами этих явлений в южных и юго-восточных районах могут быть недостаточная влажность и быстрое высыхание верхнего слоя почвы, повреждение проростков и всходов вредителями (проволочником, блошками, шведской и гессенской мухами), а в северных районах – повышенная кислотность почвы и поражение болезнями (фузариозом и др.). Яровая пшеница, особенно твердая, в первый период (в фазе всходов) развивается медленно, поэтому ее посевы часто угнетают сорняки. Вегетационный период яровой пшеницы, в зависимости от сорта, районов возделывания и погодных условий, колеблется в пределах – 85-115 дней [11], [7].
Значение биологических активных веществ (БАВ) в растениеводстве
Производство зерна в любой стране мира создает экономическую базу для развития сельского хозяйства. Повышение урожайности зерновых культур и улучшение качества получаемой продукции одна из основных и главных задач растениеводства. Решение ее невозможно без освоения современных технологий возделывания сельскохозяйственных культур, неотъемлемой частью которых является применение биологических препаратов. Влияя на процессы роста и развития растений, они способны значительно повысить урожайность большинства сельскохозяйственных культур. Известно, что биологически активные препараты активизируют основные процессы жизнедеятельности растений, а именно: ускоряют передачу информации, заложенной селекционным путем, контролируют механизмы фотосинтеза, дыхания и питания растений, Под действием биологически активных препаратов происходит снижение поступления в продукцию растениеводства ионов тяжелых металлов и радионуклидов, усиливаются адаптивные возможности растений в зоне рискованного земледелия, при этом снижается влияние стрессовых факторов среды [22].
На современном этапе государством принята программа биологизации сельского хозяйства при этом особое внимание уделяется освоению и внедрению в растениеводство экологически ориентированных технологий производства и получения экологически чистых продуктов питания. Активно ведется поиск и испытания новых биологических препаратов, действие которых в малых концентрациях приводило бы к стимуляции важнейших физиолого-биохимических процессов в растительном организме.
В РФ в настоящее время зарегистрировано несколько десятков препаратов, которые имеют свойства стимуляторов роста растений и произведены на различной основе. По своей природе и механизмам действия биологические препараты могут быть различны.
Фитогормоны – органические вещества с высокой физиологической активностью, которые вырабатываются растениями. Цитокинины – вещества контролирующие процесс деления клеток. Они задерживают процесс старения листьев, им принадлежит доминирующая роль в контроле прорастания семян, деления клеток и роста побегов. Гиббереллины способствуют повышению содержания белка, крахмала и экстрактивных веществ в зерне. Данный гормон влияет на увеличение общей массы растения. Ауксины активируют рост клеток, вызывают образование корней и регулируют многие другие процессы. Абсцизовая кислота (АБК) влияет на закрытие устьиц, при этом снижая скорость испарения воды с поверхности листьев и обеспечивая в условиях засухи ее экономичное использование. Этилен – газообразный фитогормон, который играет ключевую роль в регуляции роста растений, способствующий ускорению спелости плодов (ooo-agrika.ru; dic.academic.ru).
Многими исследованиями установлено, что с помощью регуляторов роста возможно повышение урожайности сельскохозяйственных культур. Исследователи из Оренбургского ГАУ изучали предпосевную обработку семян регулятором роста Альбит. Выявлено увеличение урожайности озимой пшеницы на 3,1 ц/га. Также было изучено некорневое внесение Гуми-30, Эпина, Циркона в поздние фазы роста и развития данной культуры. В результате исследований некорневого опрыскивания наблюдалось увеличение массы зерна в колосе. Прибавка урожая составила 0,21 т с 1 га.
В Рязанском ГАУ им. П.А. Костычева установленно, что обработка вегетирующих растений яровой пшеницы биопрепаратом Агрика способствовала повышению сохранности растений. Отмечается положительное влияние препарата Агрика на формирование элементов структуры урожайности: увеличивалась длина колоса на 0,3-0,8 см, число колосков на 0,1-1,2 шт., количество зерен в колосе на 0,6-1,5 шт. Использование данного препарата привело к увеличению урожайности на 0,25 т/га (profermer.ru/zern_udobr_agrofil).
Таким образом, по сведениям литературных источников, для повышения устойчивости к неблагоприятным факторам окружающей среды и увеличения объемов производства высококачественного зерна, при возделывании яровой пшеницы целесообразно применять биологически активные препараты.
Эти вещества могут относиться как к естественным метаболитам, принимающим участие в основных биохимических процессах, так и к группе так называемых регуляторов роста. К первой группе веществ относятся такие соединения, как органические кислоты, витамины, аминокислоты и т. д. Ко второй группе веществ можно отнести регуляторы роста, которые в очень малых концентрациях – 10-5–10-8 % оказывают сильное влияние на жизнедеятельность клетки. Данная группа веществ получила название фитогормонов.
Физиологическое действие регуляторов роста крайне разнообразно: от начала созревания до активации водородной помпы, то есть это действие проявляется как на организменном, так и на клеточном уровне. На влияние данных веществ на высшие растения указывают опыты, в которых ткани растений обогащались теми или иными органическими кислотами. Физиологи проводили опыты, в которых пытались стимулировать ростовые процессы в растениях за счет экзогенного внесения биологически активных веществ. Одним из способов внесения биологически активных веществ является замачивание в их растворах. Физиологическое действие различных БАВ весьма разнообразно. Естественно, что реакция растений на обработку разными веществами различна. Так, например, обработка семян пшеницы естественным метаболитом – парааминобензойной кислотой приводит к увеличению урожайности [4], обработка мивалом приводила к стабилизации мембран в клетках [19]. Более обширные исследования посвящены действию эндогенно вносимых фитогормонов. Это объясняется тем, что проводятся попытки подбора этих веществ с тем, чтобы обеспечить высокий и стабильный урожай сельскохозяйственных культур. Кроме того, с помощью экзогенного внесения пытаются изучить различные аспекты действия фитогормонов на растения.
Роль фитогормонов особенно важна при действии на растение неблагоприятных факторов среды. Изменение фитогормонального баланса приводит к затормаживанию одних физиологических процессов и активизации других.
Физиологи изучали действие экзогенного внесения фитогормонов при стрессе. Например, изменение температуры может быть нивелировано за счёт экзогенного внесения фитогормонов [14]. Влияние органических кислот на культурные растения в настоящее время изучается российскими и зарубежными физиологами. Еще в 1933 году В.П. Филатов установил роль органических кислот, как биогенных стимуляторов. По мнению А.В. Благовещенского, при охлаждении растительных тканей, благодаря нарушению согласованности ряда физиологических процессов, происходит одностороннее и значительное накопление ряда органических кислот. Было испытано, влияние этих кислот на процесс прорастания семян Маша.
Наиболее интересным стимулятором оказалась янтарная кислота. Стимуляция роста корней Маша под влиянием янтарной кислоты в течении 24 часов приводит к увеличению длины корней на 4 мм. Замачивание семян в растворе 0,002 % в течение суток перед посевом даёт заметную прибавку урожая [4]. Таким образом, янтарная кислота, несомненно, оказывает стимулирующее действие на обмен веществ растения, которое используют в сельском хозяйстве.
Влияние неблагоприятных факторов среды на жизнедеятельность растений
Основные показатели семян – долговечность и качество находятся в прямой зависимости от таких факторов внешней среды, как температура и влажность [15], [18]. Незначительное повышение влажности хранящихся семян может отрицательно отражаться на их влажности.
Многочисленные исследования влияния температуры на жизнеспособность семян позволили установить, что положительные температуры для семян некоторых культур более благоприятны. Например, семена гречихи с влажностью 15,5 % при хранении на холоде снизили свою всхожесть на 12 % по сравнению с хранившимися в комнатных условиях [15]. Но семена большинства видов растений лучше сохраняют жизнеспособность при хранении в условиях пониженных температур.
Наибольший угнетающий эффект наблюдается при хранении семян в условиях повышенной температуры и высокой влажности воздуха [9]. Данные условия часто имеют место в период послеуборочного хранения семян до поступления зерна на сушку. При этом в бурте зерна идёт процесс самосогревания, внешним признаком которого, является энергичное повышение температуры [6]
Имеются данные о том, что при неблагоприятных факторах среды в семенах происходит распад запасных белков изменение в системе, ответственной за новообразование белков, которая играет огромную роль при прорастании семян. При длительном хранении семян происходят изменения качества и количества белков и как следствие – снижение темпов роста и многих процессов метаболизма в проростках.
Стресс у растений
Стресс у растений – это комплексная защитная реакция, включающая как неспецифические (общие для разных типов стрессоров), так и специфические компоненты [16].
Понятие «стресс» введено в науку Гансом Селье, который называл это явление также «общим адаптационным синдромом». Под стрессом обычно понимают стереотипный (примерно одинаковый у разных особей) ответ организма на разные воздействия, сопровождающийся перестройкой его защитных сил. Считается, что главная роль стресса – мобилизация сил организма в критической ситуации.
Реакция на стресс обычно комплексная и включает в себя следующие явления: повышение проницаемости и деполяризация клеточных мембран, увеличение содержания в цитоплазме ионов кальция, выход ионов калия из клеток, повышение вязкости цитоплазмы, синтез особых «стрессорных» белков, торможение роста и деления клеток, усиление дыхания, торможение фотосинтеза, увеличение продукции гормонов стресса – абсцизовой и жасмоновой кислот, этилена.
При действии стрессового фактора в клетках растений происходит повышение проницаемости мембран, деполяризация мембранного потенциала плазмалеммы; сдвиг рН цитоплазмы в сторону кислой среды, усиление поглощения О2, развитие свободнорадикальных реакций; активизация и синтез стрессовых белков; увеличение синтеза этилена и абсцизовой кислоты, торможение деления и роста, поглотительной активности клеток и др. Эти реакции направлены на защиту внутриклеточных структур и устранение неблагоприятных изменений в клетках [13].
В невысоких дозах повторяющиеся стрессы способствуют закаливанию организма, причем, во многих случаях показано, что закаливание по отношению к одному стрессовому фактору способствует повышению устойчивости организма и к некоторым другим стрессорам.
Поскольку при стрессе изменяется фитогормональный статус растений, возникла идея об искусственном, экзогенном внесении фитогормонов и биологически активных веществ (БАВ) для восстановления исходных оптимальных показателей. Довольно часто в системе наблюдалось восстановление баланса и отмечалось снижение негативного эффекта от действия стресса. Однако положительный эффект обнаруживался не всегда, одной из причин этого называлась недостаточная изученность реагентов – фитогормонов и БАВ. В настоящее время создана классификация регуляторов роста и изучаются тонкие механизмы их действия на растения [12].
Температура является для растений стрессовым фактором. Наиболее благоприятными для жизни большинства наземных организмов являются температуры +15ºС–+30 °С. Для каждого вида имеется интервал температур, когда интенсивность физиологических процессов максимальна. Большинство растений повреждается при температуре 35 °С–40 °С. В покоящемся состоянии клетки могут переносить экстремально высокие температуры.
Температура влияет на скорость диффузии, вызывает изменение структуры белковых макромолекул, в клетках изменяется текучесть и проницаемость мембран, увеличивается количество ненасыщенных фосфолипидов, происходит потеря активности связанных с мембранами ферментов и нарушение работы переносчиков электронов (Полевой, 1989).
Температура существенно влияет на водный статус растения, вызывая возникновение водного дефицита, нарушает опыление и оплодотворение, что приводит к недоразвитию семян. У злаков высокие температуры в период заложения колосков и цветков приводят к уменьшению их числа. У многих растений высокие температуры в период цветения вызывают стерильность цветков и опадание завязей.
Пути снижения негативного эффекта действия стресса
Известно, что действие теплового шока вызывает нарушения метаболизма клеток, в частности снижения активности ферментных систем. Экзогенная обработка растений биологически активными веществами может способствовать восстановлению их жизнедеятельности.
Предполагается, что экзогенное внесение этих стимуляторов роста позволит сохранить гомеостаз растения. Действительно, в литературе представлены сведения о восстановлении прорастания семян, замоченных в растворе гибберелловой кислоты и цитоникинов [5], [20].
Многочисленные работы показали, что старение клетки сопровождается нарушением работы её генного аппарата. Известно, что активность генома регулируется фитогормональным балансом клетки. В литературе представлено мало сведений о возможности активизации генома, сниженной в результате неправильного хранения семян, за счёт обработки БАВ. Однако стимулирующее действие экзогенно внесённых биологически активных веществ весьма достоверно.
Обьекты и методика исследований
Характеристика биологических препаратов
Мизорин – препарат на основе ассоциативных азотфиксаторов для повышения урожайности и улучшения качества продукции сельскохозяйственных культур. Препарат повышает устойчивость к засухе, заморозкам и другим, неблагоприятным для растений условиям. Улучшает всхожесть семян, стимулирует рост и развитие растений [24].

Агрофил – бактериальный препарат, рекомендуемый при выращивании овощных, плодово-ягодных растений и зерновых культур. Содержит бактерии рода Агробактериум, поддерживаемых в активном состоянии на специально приготовленном торфяном материале-носителе. В 1 г. Агрофила содержится не менее 10 миллиардов клеток бактерий. Агробактерии вырабатывают антибиотики, подавляющие развитие фитопатогенных грибов и бактерий. Они способны растворять труднодоступные для растений минеральные соединения почвы, выделять ростостимулирующие вещества (природные аналоги ауксинов и гетероауксинов) и витамины [22].

ПГ-5 – биологический препарат, созданный на основе высокоэффективного штамма ассоциативных азотфиксаторов. Оно основано на способности бактерий фиксировать азот атмосферы и продуцировать ростоактивирующие вещества, стимулировать естественные природные процессы. Входящие в состав препарата бактерии продуцируют высокоактивный антибиотик «флавоцин» с широким спектром действия на фитопатогенные грибы и бактерии. Препарат снижает развитие корневых гнилей, антракноза, фитофтороза и парши. Улучшает минеральное и водное питание растений, повышает устойчивость к болезням [23].
Материал и методы исследования
Для решения поставленных задач в 2014 г. на опытном поле ФГБОУ ВПО «Самарская государственная сельскохозяйственная академия» совместно с кафедрой «Лесоводство, экология и безопасность жизнедеятельности» высевалась яровая пшеница сорта Кинельская Нива семена, которой перед посевом обрабатывались биологическими препаратами. Посев проводился делянками по схеме: 1. Контроль – семена без обработки; 2. Обработка препаратом Мизорин; 3. Обработка препаратом Агрофил; 4. Обработка препаратом ПГ-5.
Площадь опытных делянок 66 м2. Непосредственно перед уборкой урожая на каждой делянке с площади 1 м2 отбирались пробные снопы. При этом растения извлекались из почвы вместе с корневой системой. Затем в лабораторных условиях определялась структура урожая каждого варианта опыта. Для этого: определялся вес снопа с каждой опытной делянки; подсчитывалось общее число стеблей в снопе и число стеблей несущих колос; измерялась длина 20 случайно выбранных стеблей, затем определялось среднее значение по каждому варианту опыта, длина 20 случайно выбранных колосьев, затем проводилось их взвешивание и определялось среднее значение по каждому варианту опыта; проводился обмолот 20 случайно выбранных колосьев, подсчитывалось число зерен по каждому колосу, выполнялось их взвешивание и определялось среднее значение; определялась масса 1000 зерен и соотношение зерно/солома в урожае.
Предпосевная обработка заключалась в замачивании семян в растворах БАВ малой концентрации в течение 60 минут. Контрольные семена замачивались в течение 60 минут в дистиллированной воде. Семена пшеницы были разделены на порции и каждая из них замачивалась в отдельном растворе, то же производилось и со стрессовыми семенами.
Для изучения ответных реакций пшеницы на тепловой стресс был заложен лабораторный опыт, включающий в себя изучение всхожести семян и определение средней массы побегов и корней после предварительной их обработки растворами биологически активных веществ. Опытные семена хранились при температуре около 200С и влажности 20 %.
Заранее были приготовлены обеззоленные фильтры определённых размеров, чтобы они подходили для чашек Петри, которые предварительно были вымыты и высушены. В каждую чашку, на фильтр, разделённый на четыре части и смоченный дистиллированной водой, правильными рядами выкладывались семена. Количество семян в одной чашке Петри равно 40. Опытные семена перед посевом подвергали термострессу – выдерживали в сушильном шкафу при температуре 40оС в течение 3 дней. Контроль составляли растения, не подвергавшиеся предпосевному температурному воздействию. Этот метод, разработанный в конце 50-х гг А. Леопольдом, применяется для моделирования неблагоприятных условий хранения зерна на току. Семена получили названия «стрессовые».
Затем семена заливались водными растворами биологически активных веществ (Мизорин, Агрофил, ПГ-5). Часть семян, как в контроле, так и в опыте, заливалась дистиллированной водой. Инкубация проводилась в чашках Петри, в темноте, при комнатной температуре. На 3 сутки осуществлялся подсчёт прорастания семян. Проросшими принимались семена, имеющие длину стебля более 1 см и длину корня более 1,5 см. При подсчёте находилось среднее арифметическое (статистический подсчёт). С контролем производились те же подсчёты.
Метрические параметры проростков подсчитывались стандартными методами. Для взвешивания корневой части и побегов использовались торсионные весы. По результатам исследований полученные данные заносились в таблицы и составлялись графики.
Результаты исследований
Изучение и описание ответных реакций пшеницы на тепловой стресс
Особый интерес представляло выяснение влияния теплового стресса различной интенсивности на культурные растения (пшеницу). На рис. 1 отражается данные закономерности. Исследования первых этапов прорастания семян показывают, что время воздействия высокой температуры оказывает значительное действие на физиологические процессы и из выбранных вариантов наиболее приемлемым для дальнейших опытов является трёхсуточный тепловой стресс.
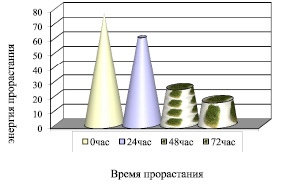
Рис. 1. Изменение энергии прорастания пшеницы
Полученные данные демонстрируют воздействие трёхсуточного теплового стресса на энергию прорастания пшеницы. Чем длительнее тепловой стресс, тем более низкая всхожесть пшеницы. На третьи сутки проращивания энергия прорастания снижалась в 4,6 раза (с 76,7 % до 16,7 %).
В ходе работы интересно было исследовать воздействие теплового стресса на линейные размеры проростков пшеницы. Известно, что под воздействием стрессовых факторов снижается интенсивность физиологических процессов в растениях, что отражается в их линейных размерах (табл. 1).
Таблица 1
Изменение длины корня и побега у проростков пшеницы
|
Срок действия высокой температуры (час) |
Вес корня |
Вес побега |
||
|
см |
%К* |
см |
%К* |
|
|
0 |
5,5 |
100 |
3,7 |
100 |
|
24 |
2 |
36 |
1,6 |
43 |
|
48 |
1,7 |
30,7 |
1,5 |
40,5 |
|
72 |
1,4 |
25,4 |
1,1 |
29,7 |
Примечание. * за контроль приняты растения, не подвергнутые действию теплового стресса.
Под действием 1, 2-х, 3-х дневного стрессов размер корней пшеницы снижается с 5,5см до 2; 1,7; 1,4см, что составляет 36 %; 30,7 %; 25,4 % соответственно к контролю. Та же тенденция прослеживается при изменении линейных размеров побегов. Снижение размеров под влиянием одного; двух; трёх суточных стрессов идёт с 3,7 до 1,6; 1,5; 1,1см соответственно (43 %; 40,5 %; 29,7 % по отношению к контролю).
Итак, результаты данных исследований показали, что наиболее негативно влияет на растение 3х суточный стресс, снижая все показатели (всхожесть, энергию прорастания, размеры, массу) по сравнению с контролем (за контроль приняты растения, не подвергнутые действию БАВ).
Влияние предпосевного замачивания семян в растворах БАВ на энергию прорастания и всхожесть проростков
Были проведены опыты по изучению действия биологически активных веществ (Мизорин, Агрофил, ПГ-5) на растения подверженных и не подверженных действию теплового стресса.
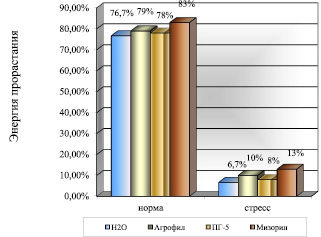
Рис. 2. Изменение энергии прорастания зерновок пшеницы под влиянием теплового стресса и обработки БАВ
Данные показывают, что введение биологических активных веществ, особенно Мизорина, увеличивает энергию прорастания семян, не подвергнутых действию теплового стресса, тогда как семена, подверженные действию теплового стресса и обработанные БАВ, наоборот, снижают энергию прорастания.
Таким образом, явно проявляется положительное влияние данных добавок на постстрессовую реакцию пшеницы: они не позволяют данному сорту резко снизить энергию прорастания в ответ на действие высокой температуры. В нормальных условиях данные биологически активные вещества также оказывают положительное влияние на энергию прорастания семян данного сорта пшеницы.
Выход фитомассы и характер кущения растений в результате обработки семян БАВ
Исследованиями установлено, что наибольший вес снопа был получен в варианте, где семена яровой пшеницы перед посевом обрабатывались биологическим препаратом Мизорин – 670 г. Это на 28,8 % больше, чем в контрольном варианте. В вариантах с ПГ-5 и Агрофилом вес снопа был соответственно на 90 г и 70 г меньше, однако и в этом случае снопы с этих посевов оказались на 11,5 % и 15,4 % тяжелее контрольного снопа (табл. 2).
Таблица 2
Фотометрические параметры посевов
|
Показатели |
Контроль |
ПГ-5 |
Мизорин |
Агрофил |
|
Вес снопа, г |
520 |
580 |
670 |
600 |
|
Число стеблей, шт. |
559 |
682 |
840 |
768 |
|
Число стеблей с колосом, шт. |
266 |
310 |
350 |
320 |
|
Продуктивная кустистость, шт. |
2,1 |
2,2 |
2,4 |
2,3 |
Подсчет числа стеблей показал, что их наибольшее количество – 840 штук на 1 м2 имеет посев, где семена обрабатывались Мизорином. В снопе контрольного посева число стеблей оказалось 550 шт. или в 1,5 раза меньше. На 22,0 % и больше чем в контрольном варианте было стеблей в посеве с применением ПГ-5 и на 37,4 % – в варианте с Агрофилом.
Очень важно, чтобы как можно больше стеблей формировали колос, поскольку это определяет урожайность посевов. Опытами установлено, что применение биологических препаратов способствует увеличению числа стеблей образующих колос в среднем на 16,5-31,6 %. По нашему мнению это связано с лучшим обеспечением растений, обработанных вариантов, необходимыми элементами питания. Поскольку бактерии, нанесенные перед посевом на семена, размножаясь, создают колонии, активно заселяющие корневые системы растений. При этом, лучше подходит к яровой мягкой пшенице бактерии, содержащиеся в препарате Мизорин. Поскольку применение данного препарата обеспечивает получение максимального количества колосьев на 1 м2 – 350 шт.
Анализ характера кущения пшеницы показал, что в кусте злакового растения контрольного посева в среднем из 5,5 стеблей только 2,1 стебля несут колос. Применение биологических препаратов способствует повышению продуктивной кустистости в среднем на 4,7-14,3 %.
Таким можно сделать заключение, что применение биологических препаратов ПГ-5, Мизорин и Агрофил в среднем на 11,5-28,8 % увеличивает выход надземной фитомассы с 1 м2 посева, на 22,0-50,0 % повышает общее число стеблей в посеве и на 16,5-31,6 % число стеблей образующих колос. При этом максимальная эффективность отмечается при предпосевной обработке семян Мизорином.
Изменение высоты стеблей и длины колоса под воздействием БАВ
Измерения в опытах показали, что наиболее высокорослые растения образуются на делянке с применением Мизорина в среднем 85,2 см. Близко к ним находятся растения посева с Агрофилом – 85,0 см, а также варианта с ПГ-5 – 84,7 см. Это в среднем на 9,4-9,7 см больше высоты контрольных растений (табл. 3).
Таблица 3
Длина стеблей и колоса
|
Показатели |
Контроль |
ПГ-5 |
Мизорин |
Агрофил |
|
Длина стеблей, см |
75.3 |
84.7 |
85.2 |
85,00 |
|
Длина колоса, см |
5.5 |
6.2 |
6.7 |
6,0 |
По нашему мнению увеличение высоты растений в посевах, где применялись биологические препараты, вызвано тем, что колонии микроорганизмов улучшают обеспечение растений в первую очередь азотом, который контролирует ростовые процессы в растениях.
Измерения длинны колосьев так же показало, что в снопах, отобранных с делянок, где применялись биологические препараты, они имеют большую длину в среднем на 0,5-1,2 см. При этом более длинные колосья были в посеве с применением Мизорина в среднем 6,7 см.
Таким образом, можно сделать заключение, что предпосевная обработка семян яровой пшеницы увеличивает высоту стеблей в среднем на 9,4-9,7 см, а длину колоса на 0,5-1,2 см. Максимально высокие растения с длинным колосом образуются при применении препарата Мизорин.
Влияние БАВ на количество зёрен пшеницы и их вес
Подсчеты обмолоченного зерна показали, что наибольшее его количество имеют колосья варианта с Мизорином в среднем на 1 колос – 29,1 шт., это на 11,6 шт. или 66,3 % больше контрольного показателя (табл. 4).
Таблица 4
Элементы продуктивности яровой пшеницы
|
Показатели |
Контроль |
ПГ-5 |
Мизорин |
Агрофил |
|
Количество зерен в колосе, шт. |
17.5 |
23.6 |
29.1 |
24,5 |
|
Вес зерен с 20 колосьев, г |
65 |
80 |
110 |
90 |
|
Вес 1000 зерен, г |
38,4 |
39,9 |
42,1 |
40,0 |
Вес зерна из 20 колосьев данного варианта равнялся 110 г, что почти в 1,7 раза больше веса зерна контрольных колосьев. Существенная прибавка отмечалась и в посевах с применением ПГ-5 и Агрофил. По числу зерен она составляла соответственно 34,8 % и 40,0 %, а их весу 23,1 % и 38,4 %.
Установлено, что наиболее полновесное, выполненное зерно с массой 1000 зерен – 42,1 г формируется в посевах с Мизорином, это на 3,7 г больше, чем в контрольном посеве. В вариантах с ПГ-5 и Агрофилом прибавка абсолютного веса 1000 зерен составляла соответственно 1,5 г и 1,6 г.
Таким образом, можно сделать заключение, что обработка семян биологическими препаратами на 34,8-66,3 % увеличивает количество зерен в колосе, на 23,1-70,0 % вес зерна и 3,9-9,6 % вес 1000 зерен. При этом максимальный эффект достигается при использовании Мизорина.
Выводы
По результатам проведенных исследований можно сделать следующие выводы:
1. Применение биологических препаратов ПГ-5, Мизорин и Агрофил в среднем на 11,5-28,8 % увеличивает выход надземной фитомассы с 1 м2 посева, на 22,0-50,0 % повышает общее число стеблей в посеве и на 16,5-31,6 % число стеблей образующих колос. Предпосевная обработка семян яровой пшеницы биологическими препаратами увеличивает высоту стеблей в среднем на 9,4-9,7 см, а длину колоса на 0,5-1,2 см, увеличивает количество зерен в колосе, на 23,1-70,0 % вес зерна и 3,9-9,6 % вес 1000 зерен.
2. Воздействие теплового стресса оказывает воздействие на энергию прорастания и линейные размеры проростков пшеницы.
3. Предпосевная обработка семян, особенно Мизорином, позволила снизить негативный эффект теплового стресса.
Библиографическая ссылка
Абрамова А.С. ВЛИЯНИЕ БИОЛОГИЧЕСКИХ ПРЕПАРАТОВ НА СТРУКТУРУ УРОЖАЯ ЯРОВОЙ МЯГКОЙ ПШЕНИЦЫ В УСЛОВИЯХ ДЕЙСТВИЯ СТРЕССА // Старт в науке. 2019. № 2-5. ;URL: https://science-start.ru/ru/article/view?id=1527 (дата обращения: 01.04.2026).
