Мир кристаллов – это сказочно красивый мир. Они завораживают своим блеском, многообразием цвета и форм.
Мне всегда было интересно рассматривать различные камни. А недавно в магазине я увидела набор для выращивания кристалла и мне стало интересно, из чего же еще можно вырастить кристаллы в домашних условиях и какие они бывают.
Перед исследованием я ознакомилась с литературой, чтобы иметь представление о предмете исследования.
В основе работы лежит утверждение, что в домашних условиях можно вырастить кристаллы.
Объектом моего исследования является изучение кристаллов и способов их выращивания.
Цель моего исследования: вырастить кристаллы в домашних условиях.
Задачи:
? познакомиться с научно-популярной литературой по данной теме
? изучить технику выращивания кристаллов
? познакомиться с разновидностями кристаллов
? узнать, какое значение имеют кристаллы в жизни человека
Гипотеза исследования: образование кристаллов зависит от условий окружающей среды, в частности от температуры.
Кристалл
Криста?ллы (от греч. κρ?σταλλος, первоначально – лёд, в дальнейшем – горный хрусталь, кристалл) – твёрдые тела, в которых атомы расположены закономерно, образуя трёхмерно-периодическую пространственную укладку – кристаллическую решётку. (рис. 1)

Рис. 1 Модель кристаллической решётки
Кристаллы – это красивые редко встречающиеся камни.
Они бывают прозрачные, различных цветов, форм и размеров. Собранные в музее, они радуют глаз.


Всё сказанное действительно справедливо, но… кристаллы – совсем не музейная редкость. Кристаллы окружают нас повсюду. Твёрдые тела, из которых мы строим дома и делаем станки, вещества, которые мы употребляем в быту, – почти все они относятся к кристаллам.
Песок и гранит, поваренная соль и сахар, алмаз и изумруд, медь и железо – всё это кристаллические тела.

В природе существуют сотни веществ, образующих кристаллы. Вода – одно из самых распространенных из них. Замерзающая вода превращается в кристаллы льда или снежинки.

Виды кристаллов
Следует разделить идеальный и реальный кристаллы.
Идеальный кристалл
Является, по сути, математическим объектом, лишённым любых дефектов строения, а также имеющим полную, свойственную ему симметрию, идеализированно ровные гладкие грани.
На рис. 2 представлено несколько многогранников. Их очертания очень совершенны, как говорят, идеально правильны.
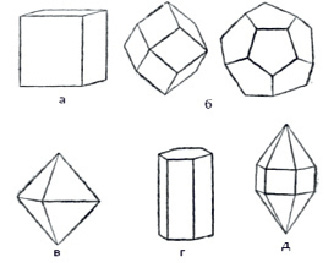
Рис. 2. Многогранники: а – куб; б – октаэдр; в – два додекаэдра – слева ромбододекаэдр,
справа пентагондодекаэдр; г – шестигранная призма; д – сочетание призмы
с двумя шестигранными пирамидами
В чём заключается совершенность изображённых тел, заслужившая для них название идеально правильных?
Реальный кристалл
Всегда содержит различные дефекты внутренней структуры решетки, искажения и неровности на гранях и имеет пониженную симметрию многогранника вследствие специфики условий роста, неоднородности питающей среды, повреждений и деформаций. Реальный кристалл не обязательно обладает кристаллографическими гранями и правильной формой, но у него сохраняется главное свойство – закономерное положение атомов в кристаллической решётке.
Методы выращивания кристаллов
Существует несколько способов выращивания кристаллов.
? Охлаждении
? Выпаривание
? Выплавка
Почти любое вещество может при известных условиях дать кристаллы. Кристаллы можно получить из раствора или из расплава данного вещества, а также из его паров.
Начните растворять в воде столовую соль или сахар. Не любое количество удастся растворить. При комнатной температуре (20 °С) вы сумеете растворить в гранёном стакане 70 граммов соли. Дальнейшие добавки соли растворяться не будут и улягутся на дне в виде осадка.


Рис. 3
Раствор, в котором дальнейшее растворение уже не идёт, называется насыщенным. Если изменить температуру, то изменится и степень растворимости вещества. Всем хорошо известно, что большинство веществ горячая вода растворяет значительно легче, чем холодная.
Представьте себе теперь, что вы приготовили насыщенный раствор, скажем, сахара при температуре 30 °С и начинаете охлаждать его до 20 °С. При 30 °С вы сможете растворить в 100 граммах воды 223 грамма сахара, при 20 °С растворяется 205 граммов. Тогда при охлаждении от 30 °С до 20 °С 18 граммов окажутся «лишними» и, как говорят, выпадут из раствора. Итак, один из возможных способов получения кристаллов состоит в охлаждении насыщенного раствора.
Можно поступить и иначе. Приготовьте насыщенный раствор соли и оставьте его в открытом стакане. Через некоторое время вы обнаружите появление кристалликов. Почему же они образовались? Внимательное наблюдение покажет, что одновременно с образованием кристаллов произошло ещё одно изменение – количество воды убыло. Вода испарилась, и в растворе оказалось «лишнее» вещество. Итак, другой возможный способ образования кристаллов – это испарение раствора.
Выращивание кристаллов
в домашних условиях
Мы приготовили насыщенные растворы соли, сахара и медного купороса при температуре 100 °С опустили в них деревянные палочки и начали их охлаждать до 20 °С. (24.03.2017 г.)


Рис. 4
При охлаждении часть вещества оказалась «лишней» и выпала из раствора.
Затем мы поставили растворы на подоконник и начали наблюдать, но решили заменить палочки на затравку и шерстяную веревку.
Через некоторое время мы обнаружили появление кристалликов. Почему же они образовались? Внимательное наблюдение показало, что количество воды уменьшилось. (20.04.2017 г.)

Рис. 5
Вода испарилась, и в растворе оказалось «лишнее» вещество.
Как же происходит образование кристаллов из раствора?
Мы сказали, что кристаллы «выпадают» из раствора; надо ли это понимать так, что месяц кристалла не было, а в одно какое-то мгновение он вдруг сразу возник? Нет, дело обстоит не так: кристаллы растут.
Не удаётся, разумеется, обнаружить глазом самые начальные моменты роста. Сначала немногие из беспорядочно движущихся молекул или атомов растворённого вещества собираются в том примерно порядке, который нужен для образования кристаллической решётки. Такую группу атомов или молекул называют зародышем.
Опыт показывает, что зародыши охотнее образуются при наличии в растворе каких-либо посторонних мельчайших пылинок. Всего быстрее и легче кристаллизация начинается тогда, когда в насыщенный раствор помещается маленький кристалл-затравка. При этом выделение из раствора твёрдого вещества будет заключаться не в образовании новых кристалликов, а в росте затравки.
Рост зародыша не отличается, конечно, от роста затравки. Смысл использования затравки состоит в том, что она «оттягивает» на себя выделяющееся вещество и препятствует, таким образом, одновременному образованию большого числа зародышей. Если же зародышей образуется сразу много, то они будут мешать друг другу при росте и не позволят нам получить крупных кристаллов.
Как распределяются на поверхности зародыша новые порции атомов или молекул, выделяющихся из раствора?
Опыт показывает, что рост зародыша или затравки заключается как бы в перемещении граней параллельно самим себе в направлении, перпендикулярном грани. При этом углы между гранями остаются постоянными.
При наблюдении за ростом кристаллов поражает основная особенность роста – параллельное перемещение граней. Получается так, что выделяющееся вещество застраивает грань слоями; пока один слой не достроен, следующий строиться не начинает.
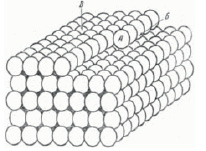
На Рис. 6 показана «недостроенная» упаковка атомов. В каком из обозначенных буквами положений прочнее всего будет удерживаться новый атом, пристроившись к кристаллу? Без сомнения, в А, так как здесь он испытывает притяжение соседей с трёх сторон, тогда как в Б – с двух, а в В – только с одной стороны. Поэтому сначала достраивается столбик, затем вся плоскость, и только потом начинается укладка новой плоскости.
Заключение
Выращивание кристаллов – очень интересный и увлекательный процесс. В результате проведенных исследований гипотеза полностью подтверждается: нам удалось вырастить кристаллы поваренной соли, сахара и медного купороса в домашних условиях.



При выполнении опытов я сталкивалась с некоторыми трудностями.
В результате опыта я пришла к выводу, что, чем насыщеннее раствор, тем быстрее вероятность образования кристалла. Если раствор охлаждать недостаточно медленно, то это приведет к образованию друзы (сростка кристаллов), т.к. его молекулы не успеют построить правильный кристалл. А при слишком резком охлаждении образуется аморфное (стеклообразное) состояние вещества.
Итак, выводы по работе:
? при благоприятных условиях поваренная соль, сахар, медный купорос принимают форму кристаллов;
? кристаллы различных веществ имеют разную форму;
? на форму кристаллов оказывает влияние температура;
? кристаллы различных веществ имеют различные свойства (одни кристаллы окрашиваются, другие – бесцветны; одни кристаллы растут хорошо, другие плохо);
? быстрее и легче кристалл растёт тогда, когда в насыщенный раствор помещается кристалл – «затравка».
Исследовательская работа мне очень понравилась. Узнала много интересного, познавательного. Но самое главное – самостоятельно вырастила кристаллы соли, сахара и медного купороса в домашних условиях.
Библиографическая ссылка
Палкина Л.А. КРИСТАЛЛЫ // Старт в науке. 2018. № 4-1. ;URL: https://science-start.ru/ru/article/view?id=1031 (дата обращения: 13.07.2025).
